Introdução
A terapia antirretroviral (TARV) atual representa um avanço impressionante ocorrido nas duas últimas décadas. A partir da monoterapia com a zidovudina, ainda nos anos 1980, drogas e classes novas e progressivamente mais potentes e seguras foram sendo introduzidas na prática clínica, com benefícios que se traduziram em níveis de sucesso virológico crescentes e duradouros, transformando uma epidemia letal em mais uma doença controlável.1 Esses benefícios se refletem em maior expectativa de vida para os infectados pelo HIV, com mais qualidade e segurança.2
Atualmente, dispomos de quase três dezenas de drogas ARV licenciadas para uso clínico, distribuídas em quatro grandes classes: os inibidores da transcriptase reversa do HIV-1 análogos de nucleosídios (ITRN) e não nucleosídios (ITRNN), os inibidores da protease viral (IP), os inibidores de entrada e, finalmente, os inibidores da integrase (INI), a última classe de ARV a ser introduzida na prática clínica. Três drogas em uso clínico compõem essa classe: raltegravir (RAL) – primeiro INI a ser utilizado no Brasil, disponível na rede pública –, elvitegravir (EVG) – não disponível em nosso meio -, e o mais recente membro, o dolutegravir (DTG) – aprovado para uso em nosso país, e que em breve deverá estar disponível na rede pública.
A classe dos INI tem se tornado referência para a TARV, desde que as principais diretrizes internacionais a elegeram como classe preferencial para compor a primeira linha de tratamento. Esse movimento teve início nos primeiros meses de 2015, quando as recomendações do U.S. Department of Health and Human Services (DHHS, Departamento de Saúde e Serviços Humanos dos Estados Unidos) foram atualizadas, e apenas esquemas baseados em INI ou IP/r (nesse caso, apenas o darunavir/ritonavir – DRV/r – foi escolhido) foram recomendados para início da TARV. Essa posição foi rapidamente secundada por outras diretrizes internacionais, e algumas (Espanha, por exemplo) passaram a recomendar apenas esquemas baseados em INI como opção preferencial para início de terapia.3,4 A tabela 1 mostra as recomendações mais recentes do DHHS.
Evidências que levaram às mudanças das recomendações para terapia inicial
Diversas razões contribuíram para essa mudança nos paradigmas existentes até então, que orientavam esquemas baseados em ITRNN, em IP/r e nos próprios INI. Em primeiro lugar, estudos mais recentes comparando esquemas baseados em INI com aqueles baseados em outras classes trouxeram resultados favoráveis aos INI, em sua maioria, como mostraremos a seguir.
O estudo STARMRK foi o primeiro a mostrar que esquemas baseados em INI (RAL) eram superiores àqueles baseados em efavirenz (EFV), até então o “padrão ouro” da TARV.
Eficácia virológica dos INI na terapia inicial, comparados a drogas de outras classes
O estudo STARMRK foi o primeiro a mostrar que esquemas baseados em INI (RAL) eram superiores àqueles baseados em efavirenz (EFV), até então o “padrão ouro” da TARV.5 Resultados semelhantes foram observados para comparações entre esquemas baseados em EVG versus EFV, nos quais o INI mostrou-se não inferior ao EFV.6 Finalmente, o estudo SINGLE comparou DTG com EFV, e novamente demonstrou-se superioridade do INI comparado ao ITRNN.7 Nesse estudo, 90% dos pacientes que utilizaram DTG e tinham carga viral (CV) basal < 100.000 cópias/mL apresentavam supressão da viremia plasmática (CV < 50 cópias/mL) após um ano de tratamento, contra 83% no grupo que utilizou EFV (p < 0,05). Para pacientes com CV basal > 100.000 cópias/mL os resultados foram semelhantes, com 83% dos pacientes no braço DTG apresentando CV indetectável, contra 76% no braço que utilizou EFV (p < 0,005). A comparação entre INI e IP mostrou resultados semelhantes: o EVG não foi inferior ao atazanavir/r (ATV/r) no tratamento de pacientes virgens de TARV.8
Por outro lado, o DTG mostrou superioridade na comparação com DRV/r no estudo FLAMINGO. Quase 500 pacientes foram alocados em braços para tratamento com esquemas contendo DRV/r ou DTG, ambos acompanhados de dois ITRN. Após 48 semanas, 90% dos pacientes no braço que utilizou DRV/r mantinham CV < 50 cópias/mL contra 83% no grupo que usou DRV/r (p = 0,02). Essa diferença aumentou até a semana 96 (80% versus 68% para os braços DTG e DRV/r, respectivamente, p = 0,002) e foi mais acentuada nos pacientes que apresentavam CV basal > 100.000 cópias/mL (82% versus 52%).9
No estudo ACTG 5257, a comparação foi feita entre esquemas baseados em ATV/r, DRV/r e RAL. As três drogas apresentaram eficácia virológica similar.10 Finalmente, quando comparados dois INI (RAL versus DTG) para tratamento de pacientes virgens de terapia (estudo SPRING-2), observou-se resposta virológica (CV < 50 cópias/mL) similar para DTG (81%) e RAL (76%) após um ano de seguimento (p > 0,05).11
Portanto, do ponto de vista da eficácia virológica, os INI mostraram desempenho similar ou superior a todos os comparadores utilizados em estudos clínicos, reafirmando a eficácia de esquemas ARV baseados em drogas dessa classe para tratamento de pacientes virgens de TARV.
Uso dos INI na terapia de resgate
O estudo BENCHMRK foi um divisor de águas na terapia de resgate, ao demonstrar que pacientes fortemente experimentados à TARV, com complexos perfis de resistência genotípica do HIV-1, podiam ser tratados com sucesso combinando uma droga nova (RAL), primeiro representante da classe dos INI, com DRV/r e/ou enfuvirtida (ENF) e terapia de base otimizada. As altas taxas de sucesso virológico nesse tipo de paciente foram surpreendentes.12 Após 96 semanas de seguimento, 57% dos pacientes em uso de RAL mostravam CV indetectável, contra apenas 26% no grupo que utilizou placebo.
O mesmo foi observado no estudo TRIO, com resultados ainda mais favoráveis. Pacientes com resistência a múltiplas drogas foram tratados com a combinação de RAL + DRV/r + etravirina (ETV), e após 48 semanas de seguimento observou-se que 86% deles apresentavam CV indetectável.13
O DTG foi comparado ao RAL para pacientes em falha à terapia anterior, mas virgens de uso de INI, no estudo SAILING. Após um ano de seguimento, observou-se superioridade na eficácia do DTG, com 71% dos pacientes que utilizaram a droga apresentando CV indetectável, enquanto no braço RAL essa proporção caía para 64% (p = 0,003). Não houve diferença na frequência de eventos adversos para os dois grupos.13
Outro estudo com braço único (VIKING 3) utilizou esquemas baseados em DTG (base otimizada com pontuação geral de suscetibilidade > 1) para tratamento de pacientes experientes e com resistência prévia a RAL ou EVG. Após 48 semanas, 63% dos pacientes apresentavam CV indetectável.14
O uso de RAL nos estudos citados não mostrou qualquer impacto dessa droga sobre a densidade mineral óssea (DMO).
Segurança e tolerabilidade dos INI
Outro ponto importante quando se trata da escolha da TARV inicial diz respeito à segurança e tolerabilidade das drogas utilizadas. Nas avaliações de eficácia dos principais estudos clínicos, a taxa de resposta geralmente é avaliada pela “intenção de tratar”, o que significa que dados ausentes ou mudanças de tratamento por qualquer razão são considerados como falha à terapia em uso. Isso explica por que em muitos estudos as taxas de supressão virológica são semelhantes, mas uma droga é considerada mais eficaz, devido, principalmente, ao seu perfil de tolerabilidade. Nesse quesito, novamente os INI se destacam como drogas ARV seguras e bem-toleradas.
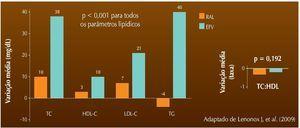
Um dos principais problemas associados à TARV é o impacto de muitos ARV sobre o metabolismo de lipídios e da glicose (resistência à insulina). No estudo STARTMRK, o RAL apresentou um impacto sobre os níveis séricos de lípides significativamente menor que o observado para o EFV (fig. 1).1
Figura 1 STARTMRK: Alterações nos lípides desde baseline até a semana 96.
Achados divergentes foram observados no estudo PROGRESS, que comparou esquemas utilizando liponavir (LPV)/r + RAL versus LPV/r + 2 ITRNs.15 O grupo que utilizou o RAL apresentou maiores elevações nos níveis séricos de colesterol total e triglicérides, em comparação ao grupo que utilizou 2 ITRNs. No estudo SPARTAN (interrompido por altas taxas de hiperbilirrubinemia), no qual o RAL foi combinado ao ATV/r e comparado a esquemas com ATV/r e 2 ITRNs, não foram observadas diferenças entre os grupos no tocante às alterações lipídicas.16
Outro estudo que mostra impacto maior sobre o metabolismo lipídico na associação RAL e IP foi o NEAT 001/ ANRS114, que comparou pacientes tratados com DRV/r + RAL versus DRV/r + tenofovir (TDF) + emtricitabina (FTC). Embora a eficácia virológica global tenha sido semelhante para ambos os braços, observou-se elevação significativamente maior de lípides séricos no grupo RAL + DRV/r. Observou-se ainda que pacientes no grupo RAL apresentaram eficácia virológica inferior quando a CV basal ultrapassava 100.000 cópias/mL ou CD4 basal < 200 células/mm3.17
O DTG mostrou perfil semelhante, com impacto significativamente inferior ao provocado pelos esquemas baseados em DRV/r, no estudo FLAMINGO, que comparou esquemas baseados nessas duas drogas para tratamento de pacientes virgens de TARV.9
O estudo ACTG 5257 propiciou a oportunidade de comparação de esquemas baseados em três drogas de duas classes diferentes, IPs (ATV/r ou DRV/r) vs. INI (RAL) Além disso, avaliou a associação desses ARV com duas duplas de ITRNs, abacavir (ABC) + lamivudina (3TC) e TDF + FTC. Embora não tenham sido detectadas diferenças em termos de eficácia virológica entre os braços (RAL = 94%; DRV/r = 89%; ATV/r = 88%), a eficácia foi afetada pelo perfil de tolerabilidade, com melhor desempenho de RAL, seguido por DRV/r, e finalmente ATV/r (RAL = 80%; DRV/r = 73%; ATV/r = 63%).10
Por outro lado, em estudos de switch observamos redução significativa nos níveis de lípides na troca de esquemas baseados em LPV/r para RAL, como o SWITCHMRK e SPIRAL.18,19 O estudo SINGLE confirma que o DTG teve desempenho favorável nesse item, em comparação ao EFV, em pacientes virgens de terapia.7 No estudo SPRING, a comparação entre esquemas baseados em RAL e DTG mostrou perfil semelhante entre as duas drogas para tratamento de pacientes virgens de TARV.11
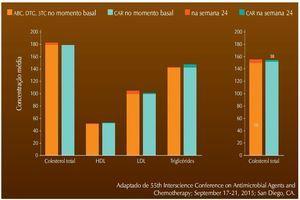
Os achados foram semelhantes no estudo STRIVIING, no qual os pacientes tinham esquemas baseados em diversas drogas trocados por DTG+3TC+ABC. Observouse redução significativa nos níveis séricos de colesterol e triglicérides, como observado na figura 2.20
Figura 2 Mudança de lípides em jejum, desde o momento basal.
O perfil de tolerabilidade se mantém quando outros parâmetros são avaliados. O RAL mostrou incidência significativamente menor de eventos adversos relacionados ao sistema nervoso central no estudo STARTMRK.5
A utilização de DTG e EVG tem sido associada a alterações dos níveis séricos de creatinina, com pequeno impacto na taxa de filtração glomerular estimada. Isso ocorre pelo bloqueio provocado por essas drogas na excreção renal de creatinina, ocasionando uma elevação dos seus níveis séricos, sem que isso se relacione com alterações da função renal.21,22 Foi observado que essas alterações ocorreram precocemente no curso da terapia e não progrediram, mesmo com 144 semanas de seguimento. Na comparação entre RAL e DTG, as alterações nos níveis de creatinina foram maiores para os pacientes que utilizaram DTG.
Finalmente, o uso de RAL nos estudos citados não mostrou qualquer impacto dessa droga sobre a densidade mineral óssea (DMO). Para o DTG, as informações disponíveis indicam que não há alterações nos biomarcadores de metabolismo ósseo, mas não existem dados específicos avaliando o impacto potencial sobre a DMO.