Desde o seu aparecimento no arsenal terapêutico de tratamento para infecção por HIV, os inibidores de integrase (INI) são considerados drogas fundamentais para os esquemas de resgate, principalmente no tratamento de terceira linha, após falha das três classes mais antigas: inibidores da transcriptase reversa análogos de nucleosídeos (ITRN) e não análogos de nucleosídeos (ITRNN), e os inibidores de protease (IP).
Em nosso país, a primeira droga desta classe, disponibilizada para uso clínico, foi o raltegravir (RAL). Embora tenha se mostrado um agente antirretroviral seguro e de alta potência intrínseca desde o início de seu desenvolvimento – clinicamente caracterizada por uma queda precoce e acentuada da carga viral (CV)1 –, foi também reconhecida, a partir dos estudos de registro, a limitada barreira genética à resistência desta droga, tendo sido identificadas mutações associadas à resistência na região da integrase em um percentual significativo de pacientes que apresentavam falha terapêutica.2-4
O dolutegravir (DTG) representa uma nova geração de inibidores de integrase com melhor perfil farmacocinético, que possibilita dosagem única diária e apresenta potencial para maior barreira genética com relação à resistência.5
Estudo Sailing
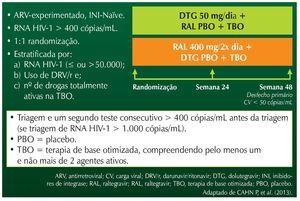
O estudo Sailing comparou o uso de dolutegravir 50 mg/dia com o uso de Raltegravir na dose habitual de 400 mg 12/12 hs, em pacientes apresentando falha virológica e sem história prévia de exposição a esta classe.6 O estudo seguiu um modelo duplo cego, placebo controlado, no qual uma das drogas era utilizada com o placebo da outra droga, em combinação com um esquema de base otimizado. Pelos critérios de inclusão, era necessária apenas a identificação de resistência a duas das classes de antirretrovirais. O número de agentes escolhidos para compor o esquema de base otimizado também era limitado a dois, e pelo menos um deles deveria ser plenamente ativo, segundo análise dos testes de resistência genotípico e fenotípico. Outro dado importante, o número de pacientes que poderiam usar darunavir (DRV) sem apresentar mutações primárias para inibidores de protease na entrada do estudo, foi limitado, para possibilitar a avaliação do efeito específico do inibidor de integrase no sucesso do esquema de resgate, uma vez que esquemas contendo darunavir na ausência de mutações com impacto na sua atividade costumam ter alta eficácia, independentemente de outros agentes usados em combinação. Também por esse motivo, a randomização do estudo adotou o critério de estratificação pelo uso de darunavir sem mutações de resistência na protease versus não uso desta droga, ou uso com mutações na protease. Outros parâmetros usados para estratificação, de forma a garantir que os dois braços fossem semelhantes em relação a aspectos significativamente associados ao sucesso terapêutico, foram a CV > 50.000 cópias/mL e o número de agentes ativos na terapia de base otimizada (2 versus < 2). O desfecho primário do estudo foi estabelecido como CV para HIV < 50 cópias/mL na semana 48 de acompanhamento. Uma visão geral do estudo está esquematizada na figura 1. O estudo foi desenhado visando demonstrar inicialmente a não inferioridade do dolutegravir, de maneira que o intervalo de confiança de 95% (IC 95%) afastasse a hipótese de que a diferença de eficácia entre o braço dolutegravir versus o braço raltegravir fosse > -12%. Caso esse objetivo fosse atingido, seria então testada a hipótese de superioridade do dolutergravir. Assumindo, em princípio, uma eficácia virológica prevista de 65%, para o estudo conseguir identificar essa diferença com 90% de poder, eram necessários aproximadamente 333 voluntários em cada grupo. Uma importante análise desse estudo referiu-se à seleção de cepas com mutações de resistência na integrase. O teste de resistência na integrase era feito, conforme protocolo, em todos os pacientes que atingiam a definição de falha virológica; queda < 1 log na semana 16 (desde que fosse maior do que 400 cópias/mL) e > 400 cópias/mL a partir de então.
Figura1 Desenho do estudo.6
Dos pacientes que participaram da visita inicial, 724 foram incluídos no estudo e randomizados para um dos dois braços: 360 para o braço dolutegravir e 364 para o braço raltegravir. Destes, 357 pacientes no braço dolutegravir e 362 no braço raltegravir tomaram ao menos uma dose do medicamento do estudo. Um número adicional de quatro pacientes foi excluído devido a problemas associados à violação das boas práticas clínicas em um dos centros participantes, totalizando 715 pacientes na análise primária do estudo.
As características basais dos participantes mostram que 68% eram do sexo masculino, havendo uma ampla diversidade de etnias, mas com uma predominância do vírus do subtipo B (68%), sem diferenças estatísticas entre os grupos no que diz respeito à distribuição desses parâmetros. Quase metade dos pacientes tinha história prévia de condições definidoras de AIDS, e um número semelhante apresentava resistência a pelo menos uma droga de três ou mais classes de antirretroviriais. A mediana de CD4 foi de 200 céls/mm3 (IIQ 95-366), e a mediana de carga viral foi de 4,18 log (IIQ3,45-4,84). Foi encontrada, também, uma frequência de 5% de pacientes coinfectados com o vírus da hepatite B e 11% com o vírus da hepatite C.
O teste de resistência na integrase era feito, conforme protocolo, em todos os pacientes que atingiam a definição de falha virológica.
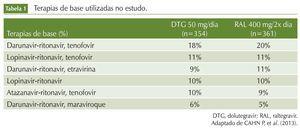
Em relação aos parâmetros utilizados para estratificação, a CV > 50.000 cópias/ mL foi encontrada em 30% dos voluntários de ambos os grupos; o escore fenotípico < 2, em 26% dos pacientes do grupo dolutegravir e em 29% do grupo raltegravir, e o uso de darunavir na ausência de mutações primárias na protease em 20% do braço dolutegravir e 21% do braço raltegravir. Um inibidor de protease reforçado com ritonavir foi utilizado em 84% dos pacientes no braço dolutegravir e 85% no braço raltegravir. Os esquemas mais utilizados nesse estudo estão demonstrados na tabela 1.
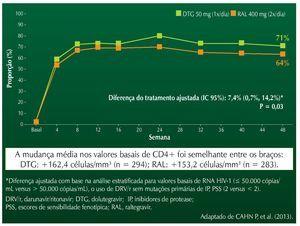
Na análise relacionada ao desfecho primário, conforme previamente demonstrado em estudos incluindo inibidores de integrase, o percentual de pacientes com supressão virológica < 50 céls/mm3 aumentou rapidamente até a semana 4, tendendo à estabilização a partir da semana 8. Na semana 48, 71% dos pacientes no braço dolutegravir e 64% dos pacientes no braço raltegravir apresentavam RNA HIV < 50 cópias/mL. A diferença a favor do dolutegravir de 7,4% com IC 95% de 0,7 a 14,2 permitiu concluir pela não inferioridade, em comparação com o raltegravir, uma vez que a margem inferior do intervalo de confiança não ultrapassou o ponto estabelecido de -12%. A superioridade pode ser demonstrada em uma análise estatística planejada previamente (p = 0,003). Os resultados de supressão viral < 50 cópias/ mL durante as 48 semanas de acompanhamento estão demonstrados na figura 2.
Figura2 Carga viral < 50 cópias/mL até 48 semanas de acompanhamento.6
É importante ressaltar que a diferença favorável ao dolutegravir, considerando a análise segundo a intenção de tratar, foi gerada principalmente pelos diferentes índices de sucesso virológico nos dois braços. De fato, a taxa de não resposta virológica no braço raltegravir foi de 28% versus 20% no braço dolutegravir. Em relação à análise por característica usada na estratificação, foi possível observar que a diferença era acentuada nos pacientes com fatores comumente associados à má resposta, como CV > 50.000 cópias/mL, quando a diferença foi bastante significativa (62% versus 47%), e não uso de darunavir ou uso na presença de mutações na protease. O único subgrupo no qual não houve diferença demonstrável entre os braços foi justamente o dos pacientes que utilizaram darunavir sem mutações primárias na protease, onde a resposta foi praticamente a mesma (69% versus 68%). Este resultado é consistente com estudos anteriores, que mostram que, na ausência de mutações primárias na protease, a resposta virológica ao esquema de resgate contendo estes agentes não parece depender significativamente da atividade dos outros componentes do esquema terapêutico. No DUET – estudo de registro do ITRNN de segunda geração etravirina, no qual o darunavir/r foi incluído no esquema de base otimizado de todos os participantes –, por exemplo,7 foi possível demonstrar que, na ausência de mutações na protease relacionadas à resistência a esta droga e considerando os pacientes que utilizaram apenas darunavir/r e ITRN, o uso da etravirina não aumentou a resposta virológica, em comparação com o placebo.8 Por outro lado, a presença de apenas uma mutação já fazia com que a resposta fosse estatisticamente superior no braço da etravirina. Embora, de maneira geral, a presença de apenas uma mutação não comprometa a atividade fenotípica do darunavir/r, é possível imaginar que reduza sua barreira genética, limitando assim a durabilidade de um esquema baseado unicamente em IP/r. Da mesma forma, a análise do estudo Second line, que comparou o uso em segunda linha do lopinavir como primeiro IP/r combinado com ITRN ou com o raltegravir, demonstrou eficácia virológica semelhante, mesmo em um contexto no qual a sensibilidade genotípica à classe dos ITRNs já estava afetada pela presença de mutações selecionadas após a falha ao esquema de primeira linha (2ITRN + 1 ITRNN).9 Na realidade, o fato mais eloquente foi o achado de maior eficácia no subgrupo em que a resistência aos ITRNs era mais expressiva.10 Isto se deu, provavelmente, porque esse parâmetro marcou um grupo de melhor adesão, uma vez que a baixa resistência encontrada em pacientes com falha terapêutica geralmente indica que o paciente não está tomando a medicação adequadamente. Todos estes dados em conjunto sugerem que, na ausência de mutações com impacto na sensibilidade ao inibidor de protease que compõe o esquema, a adesão é o único fator significativamente associado ao sucesso terapêutico.
Outra análise interessante relacionava--se ao pequeno subgrupo de pacientes que utilizou apenas ITRN no esquema de base otimizado, com 32 pacientes em cada braço. No braço dolutegravir não foi encontrada falha virológica definida pelo protocolo, enquanto no braço raltegravir, sete dos 32 pacientes apresentaram esse desfecho. Deve ser ressaltado que, dentre os 32 pacientes do braço dolutegravir, em apenas metade era possível demonstrar atividade dos dois agentes ITRN. Embora esses resultados reflitam apenas um pequeno grupo de pacientes do estudo, fica aberta uma interessante perspectiva em relação a esquemas de segunda linha sem IP/r, bem como a troca estável (switch) do IP/r para dolutegravir. Isto já foi tentado com o raltegravir no protocolo SWITCHMRK, porém sem sucesso, devido principalmente à ação limitada, em muitos pacientes do estudo, dos ITRNS que compunham o esquema de base, pela presença de mutações de resistência selecionadas em falhas virológicas anteriores à entrada no estudo.4
Os dados de segurança do estudo Sailing mostraram que a frequência de eventos adversos nos dois braços foi semelhante e, geralmente, de intensidade leve a moderada. Eventos que levaram à interrupção do tratamento foram pouco comuns. Não houve morte no braço dolutegravir, e as três que ocorreram no braço raltegravir não foram associadas aos medicamentos em uso. O número de anormalidades laboratoriais significativas (graus 3 e 4) também foi bastante reduzido em ambos os grupos e, na maior parte das vezes, essas anormalidades foram relacionadas a comorbidades, como hipertensão e diabetes. Um pequeno aumento da creatinina sérica foi encontrado em ambos os grupos na semana 2, com estabilização a partir deste ponto, consistente com o conhecimento sobre a inibição específica da secreção tubular de creatinina com o uso de dolutegravir, sem impacto sobre a função renal.11 A elevação das enzimas hepáticas > 5 x em relação aos limites superiores dos valores de referência ocorreu em 3% versus 2% nos braços dolutegravir versus raltegravir, respectivamente. Estes casos ocorreram predominantemente em pacientes coinfectados por hepatites B (HBV) e C associadas à síndrome de recuperação imunológica, especialmente quando as drogas com ação para HBV não foram utilizadas. De forma geral, este estudo reforça os dados encontrados no estudo SPRING-2, que comparou estas duas drogas para tratamento inicial com base em abacavir-lamivudina ou tenofovir--emtricitabina (TDF-FTC), segundo escolha do investigador, mostrando perfil de segurança semelhante em ambos os braços.12 De fato, este perfil favorável de segurança e tolerabilidade é uma das principais características da popularidade dos inibidores de integrase como componente de esquemas de primeira linha e é, em geral, responsável pela maior eficácia nos estudos que compararam estes medicamentos com outras classes.
Embora o sucesso do tratamento esteja sempre condicionado à adesão do paciente, após a seleção de resistência há uma perda de opções terapêuticas
Um desfecho importante, relacionado à terapia antirretroviral, diz respeito à seleção de cepas resistentes em caso de falha terapêutica. Embora o sucesso do tratamento esteja sempre condicionado à adesão do paciente, após a seleção de resistência há uma perda de opções terapêuticas, não só das medicações em uso, mas também de outras drogas das mesmas classes, uma vez que frequentemente ocorre a resistência cruzada. Neste caso, não será apenas o estímulo à adesão que não trará de volta a supressão viral adequada, fenômeno que acontece com frequência com esquemas de primeira linha contendo IP/r, mas também as opções de resgate podem ficar limitadas. O dolutegravir vem mostrando, em todas as etapas de seu desenvolvimento, um perfil diferenciado dentro da classe, uma vez que a seleção de cepas resistentes não foi encontrada até o momento em esquemas de primeira linha.12-14 Em contraste, o raltegravir costuma estar associado à seleção de mutações de resistência com alguma frequência em caso de escape virológico, e estas mutações têm impacto nas outras drogas da classe, principalmente o complexo 148H-140S, que reduz a atividade do dolutegravir,15 comprometendo a eficácia dos esquemas baseados nesta droga, mesmo quando utilizada dose dobrada deste medicamento.16 Estudos de terapia de resgate, no entanto, costumam representar um desafio à barreira genética dos medicamentos, uma vez que a atividade dos demais agentes do esquema de base otimizado está muitas vezes comprometida pela falha prévia a drogas de mesma classe. Nesse contexto, os resultados desse trabalho são muito importantes, pois é o único estudo controlado que utilizou dolutegravir em situações de resgate como primeiro agente da classe. Os dados obtidos confirmaram o perfil diferenciado da droga, uma vez que um número significativamente menor de pacientes no braço dolutegravir apresentou substituições na integrase, em comparação com o braço raltegravir (4 versus 17, p = 0,003). Em um dos quatro pacientes com mutações de resistência na integrase foi demonstrada a presença destas mutações já na entrada no estudo (148H-140S), sugerindo uso prévio da classe. Dois outros apresentavam uma substituição identificada anteriormente em estudos in vitro a 263K, que confere apenas uma discreta redução de aproximadamente duas vezes na susceptibilidade à droga, sem impacto significativo na resistência fenotípica.5 O outro paciente apresentou carga viral elevada em todas as visitas de seguimento, com presença de um polimorfismo detectado no momento da constatação da falha virológica na posição 151, mas que não comprometia a atividade de nenhum dos medicamentos conhecidos desta classe. Estes resultados estão demonstrados na tabela 2.
Assim, mesmo em um estudo no qual o dolutegravir foi utilizado como terapia de resgate combinado a medicamentos com atividade nem sempre confiável, não houve caso registrado de seleção de resistência clinicamente significativa.
Neste momento, quando o dolutegravir deve ser integrado em nossas diretrizes para tratamento antirretroviral, quais as mensagens mais importantes a serem retiradas deste estudo? Os resultados encontrados confirmam as características já conhecidas do dolutegravir, isto é, uma droga que mantém a potência reconhecidamente elevada e o perfil de segurança favorável desta classe, acrescentando, ainda, algo muito valioso: a barreira genética que forma um gargalo para seleção de cepas resistentes, papel que até o momento era desempenhado apenas pelos IP/r. Pode-se fazer, inclusive, uma analogia entre o dolutegravir e os inibidores de integrase de primeira geração – raltegravir e elvitegravir – e a relação entre os IP/r e os inibidores de protease sem reforço com ritonavir, uma vez que as mutações são selecionadas pelo dolutegravir apenas quando há falha prévia aos agentes da mesma classe. O estudo VIKING, por exemplo, que investigou o uso de dolutegravir após falha a outros inibidores de integrase – raltegravir e elvitegravir (droga não disponível no Brasil até o momento) –, mostrou que nos casos em que um perfil mutacional desfavorável estava presente no início do estudo (a combinação 148H e 140S), mutações adicionais de resistência foram selecionadas pelo uso de dolutegravir, levando a uma redução muito significativa da susceptibilidade a esta droga.13
Os resultados encontrados confirmam as características já conhecidas do dolutegravir: uma droga que mantém a potência reconhecidamente elevada, perfil de segurança favorável, a barreira genética que forma um gargalo para seleção de cepas resistentes
Neste estudo, a barreira genética se encontra, muito provavelmente, na origem da vantagem obtida pelo dolutegravir em relação à resposta virológica particularmente percebida nos pacientes com maior número de fatores desfavoráveis, como carga viral elevada e mutações de resistência na classe dos IP. Estes seriam os casos em que o dolutegravir deveria prioritariamente ser escolhido como inibidor de integrase para compor o esquema de resgate. É importante ressaltar que, nesta situação, o dolutegravir pode inclusive representar uma economia, pois reduz a necessidade de outro agente de classe nova (inibidores de entrada, ITRNN de segunda geração) no esquema, desde que o IP/r ainda seja considerado ativo.
Outro potencial que aparece neste estudo – uso em combinação com ITRN após falha ao nosso esquema preferencial de primeira linha: tenofovir/lamivudina/ efavirenz – precisa ser explorado em estudos com maior amostragem, para que possa ser avaliado mais amplamente.
Uma questão mais complexa seria a indicação de troca estável do raltegravir para o dolutegravir para aqueles pacientes que já estão em uso do primeiro em seus esquemas de resgate e apresentam carga viral suprimida. Os fatores que deveriam ser levados em conta nesta situação seriam a presença de mutações para IP e o número de drogas ativas. Se o esquema de resgate é composto por um IP-r para o qual não há mutações primárias de resistência, ou se o esquema é composto por pelo menos três drogas plenamente ativas, esta troca pode não ser necessária. Os dados do estudo BENCHMRK mostram que, na presença de duas drogas plenamente ativas com o raltegravir , o risco de seleção de cepas resistentes na falha é reduzido em 33%, em comparação com os casos em que havia menos de duas drogas ativas (75%).3
O estudo em discussão, portanto, mostra que a disponibilização do dolutegravir para uso em nosso país representa um marco importante, pelas suas características singulares, mesmo ele não sendo o primeiro agente da classe dos inibidores de integrase. Teremos, afinal, um segundo ponto de controle sobre o desenvolvimento de cepas multirresistentes e tornando possível reduzir custos relacionados à adição de novas drogas ao esquema terapêutico em que esta medicação estiver presente, e, em situações especiais, será mais seguro abrir mão dos IP/r em esquemas de resgate, mantendo a supressão viral por meio de esquemas simples e de alta eficácia.
Por último, é importante notar que, em países com recursos mais amplos, por sua elevada eficácia e excelente perfil de segurança, os inibidores de integrase já são os agentes preferenciais para construção de esquemas de primeira linha em combinação com bases de ITRN.17 À medida que os custos viabilizarem este modelo de incorporação, será possível pensar que esta passará a ser também a tendência para o nosso país. É muito importante, portanto, que saibamos usar adequadamente esta classe, para que nossos pacientes não percam a chance de se beneficiarem, no futuro, do grande avanço representado por estes agentes no tratamento das pessoas portadoras de HIV.